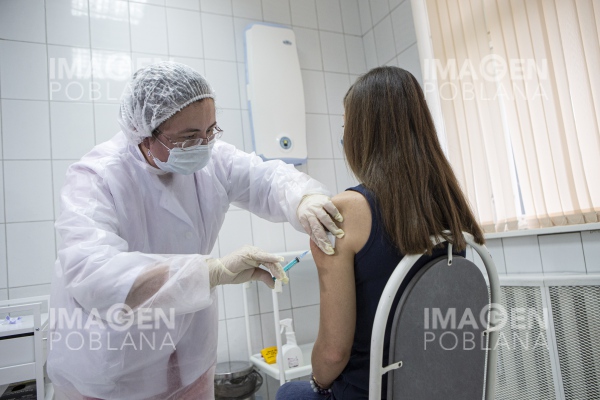
A través de un comunicado conjunto, las farmacéuticas BioNTech y Pfizer anunciaron que el 20 de noviembre de 2020 solicitaron a la FDA (Administración de drogas y alimentos) de Estados Unidos autorización de uso de emergencia para la vacuna BNT162b2 contra el COVID-19. Esto tiene el objetivo de posibilitar su aplicación a poblaciones de riesgo previo a la temporada invernal de 2020.
Tras completar las pruebas clínicas de fase 3, ambas compañías concluyeron que la vacuna BNT162b2 muestra un 95% de efectividad para generar una respuesta en el organismo contra el virus SARS-Cov-2. Detallaron que el ensayo principal estuvo respaldado por muestras adicionales de 46,000 voluntarios mayores de 18 años seleccionados de forma aleatoria, además de cien menores de 12 a 15 años.
Por otra parte, 42% de los voluntarios proviene de "contextos de diversidad étnica" y un 41% de la población probada está entre los 56 y 85 años de edad. De acuerdo con el comité interno de monitoreo de datos del estudio, no se han registrado problemas de seguridad relacionados con la vacuna.
 Según la Ley federal de Alimentos, Medicamentos y Cosméticos de Estados Unidos, la FDA está encargada de controlar y supervisar la seguridad de productos alimenticios, vacunas, dispositivos médicos, entre otros. En casos de emergencia nacional, como la declarada por el Departamento de Seguridad Nacional desde el 4 de febrero de 2020 con motivo de la pandemia de coronavirus, esta puede autorizar el uso limitado de una sustancia aún no plenamente aprobada. Basada en un criterio probabilístico, una autorización de uso de emergencia está orientada a circular productos médicos con menor evidencia científica de su efectividad.
Según la Ley federal de Alimentos, Medicamentos y Cosméticos de Estados Unidos, la FDA está encargada de controlar y supervisar la seguridad de productos alimenticios, vacunas, dispositivos médicos, entre otros. En casos de emergencia nacional, como la declarada por el Departamento de Seguridad Nacional desde el 4 de febrero de 2020 con motivo de la pandemia de coronavirus, esta puede autorizar el uso limitado de una sustancia aún no plenamente aprobada. Basada en un criterio probabilístico, una autorización de uso de emergencia está orientada a circular productos médicos con menor evidencia científica de su efectividad.
Adicional a la enviada a la FDA, BioNTech y Pfizer aseguraron que ya han enviado solicitudes a múltiples agencias de salud, específicamente la Agencia de medicamentos europea y la Agencia de regulación de productos para la salud en Reino Unido. También solicitarán aprobación en Canadá, Japón, Australia y, eventualmente, otras agencias reguladoras alrededor del globo.
Aprovechando el expertise en manufactura de mRNA de BioNTech y la cadena de logística y envío en frío de Pfizer, las farmacéuticas proyectan poder entregar 50 millones de dosis de la vacuna en 2020. De completar satisfactoriamente los procesos de regulación, y si las capacidades de distribución y manufactura lo permiten, esperan entregar 1,300 millones de vacunas para el fin de 2021.
Queda pendiente la aprobación del uso de emergencia de la nueva vacuna de Pfizer y BioNTech por parte de la FDA en Estados Unidos, además de su posible introducción en suelo mexicano de parte de la Cofepris. De acuerdo con el comunicado, se priorizará su aplicación a poblaciones de riesgo como personal médico, adultos mayores, personas inmunodeprimidas o con enfermedades graves.



